国内第三张干细胞《药品生产许可证》颁发
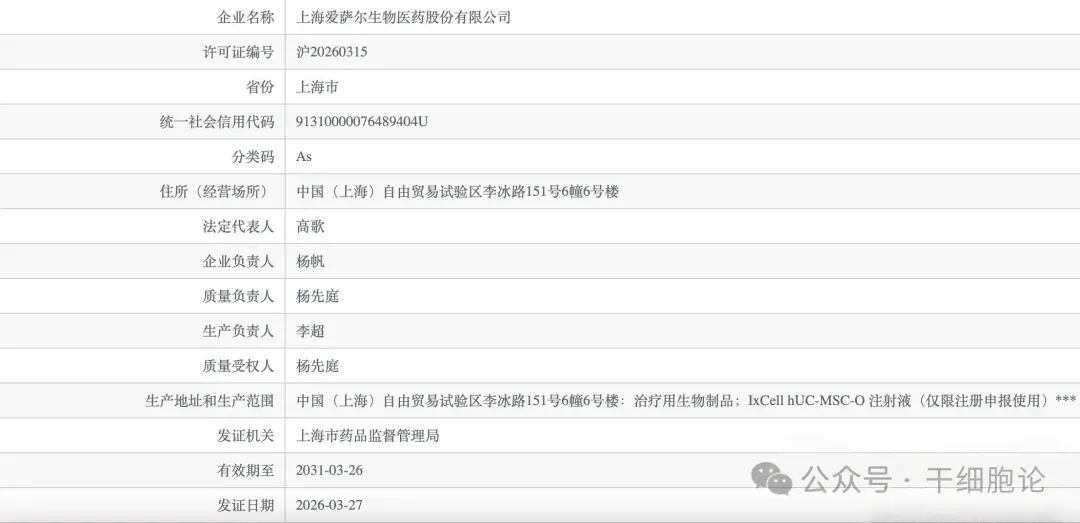
2026年3月27日,爱萨尔生物正式获得了由上海市药品监督管理局签发的干细胞《药品生产许可证》(编号:沪20260315)。根据报道,爱萨尔生物自成立以来,已完成至少7轮融资,穿越了多个资本市场周期,目前处于C+轮阶段。

这张证书不仅是国内第三张,更是上海首张,在业内激起了广泛的关注与讨论。国内第一张干细胞《药品生产许可证》,是2021年江苏药监局批给江苏拓弘的,他们的克罗恩病肛瘘在做临床III期,是国内该病种领域最快的一家。国内第二张干细胞《药品生产许可证》,是2024年5月30日北京市药品监督管理局核发的,获得方为铂生卓越生物科技(北京)有限公司,许可证编号京20240083。
干细胞治疗,尤其是针对膝骨关节炎等退行性疾病的治疗,长期以来被视为再生医学的希望,但其发展一直受制于技术标准化、质量控制和监管路径的挑战。爱萨尔生物的核心产品——人脐带间充质干细胞注射液(IxCell hUC-MSC-O),瞄准的正是膝骨关节炎这一巨大未满足的临床需求,该产品在2019年5月17日便获得IND批件,自此开启了长达近七年的潜心研发之路。
此次生产许可证的获取,首先意味着监管层面对其生产质量管理体系(符合cGMP标准)的全面认可。这证明了爱萨尔生物已经具备了稳定、可控、大规模的工业化生产能力,为产品未来上市后的供应奠定了坚实的硬件基础,解决了干细胞药物从“做出来”到“标准化生产出来”的核心瓶颈。
其次,它意味着产品上市的最后一道主要技术壁垒已被清除。新药上市需要经历临床前研究、临床试验、新药上市申请审批以及生产资质获取等多个环节。
2024年12月,该产品顺利完成全部III期患者给药,用严谨的临床数据夯实了疗效与安全性的基础;
2025年3月,又成功获批在瑞金医院海南院区开展合规收费治疗,截止目前共完成368例治疗。成为国内少数进入后期研发阶段、并率先实现合规收费的干细胞疗法之一。
展望未来,这张许可证无疑为产品的最终上市铺平了最关键的道路。它极大地缩短了获批后产品推向市场的时间,一旦NDA获得批准,生产线即可迅速启动。
当然,理性看待,这张许可证不等于立即上市,最终的NDA审评批准仍需国家药监局基于全部数据做出审慎决策,时间上仍存在一定的不确定性。
但毋庸置疑,最大的不确定性之一已经消除,新的一个具备更全面适应症的干细胞药品上市曙光已然清晰可见。
免责声明:本文来源于细胞plus,内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
