胃癌诊疗新进展:ADC药物引领科研与临床双突破,重塑消化道肿瘤治疗格局
胃癌作为全球第五大常见恶性肿瘤、我国消化道肿瘤防治的重中之重,具有起病隐匿、中晚期预后差、传统治疗疗效有限等特点,约80%患者确诊时已错失手术根治机会。
近年来,以抗体偶联药物(ADC)为核心的精准治疗领域迎来科研成果井喷+新药密集落地的双重突破,HER2、CLDN18.2两大核心靶点的ADC药物不仅完成多项关键临床研究、斩获新适应症,其耐药机制、联合治疗策略的基础科研也取得重要进展,为不同分子分型、不同分期的胃癌患者带来全新的生存希望。
01基础科研深耕
解锁ADC药物研发与耐药核心密码
ADC药物的临床突破离不开基础科研支撑,近年来针对胃癌HER2、CLDN18.2靶点机制、ADC药物作用及耐药通路的研究,为其研发和联合治疗奠定基础,推动精准治疗从“靶点选择”走向“机制优化”;同时胃微生物群在胃癌转移中的作用也被逐步揭示,为转移靶向治疗提供新方向。
靶点研究中,明确HER2在10%-20%胃癌患者中高表达,其异质性影响治疗效果;CLDN18.2在40%-60%相关患者中特异性高表达,是ADC研发最优潜力靶点,其表达水平与肿瘤恶性程度相关。此外,ADC药物“免疫原性细胞死亡”机制,为其与PD-1/PD-L1抑制剂联合治疗提供理论支撑。
2026年2月,浙江大学滕理送等团队在GUT发表的研究,揭示鲍曼不动杆菌可作为胃癌促转移因子,通过干扰NAD代谢、激活HIF-1及增强糖酵解促进转移,为转移靶向治疗提供新机制。
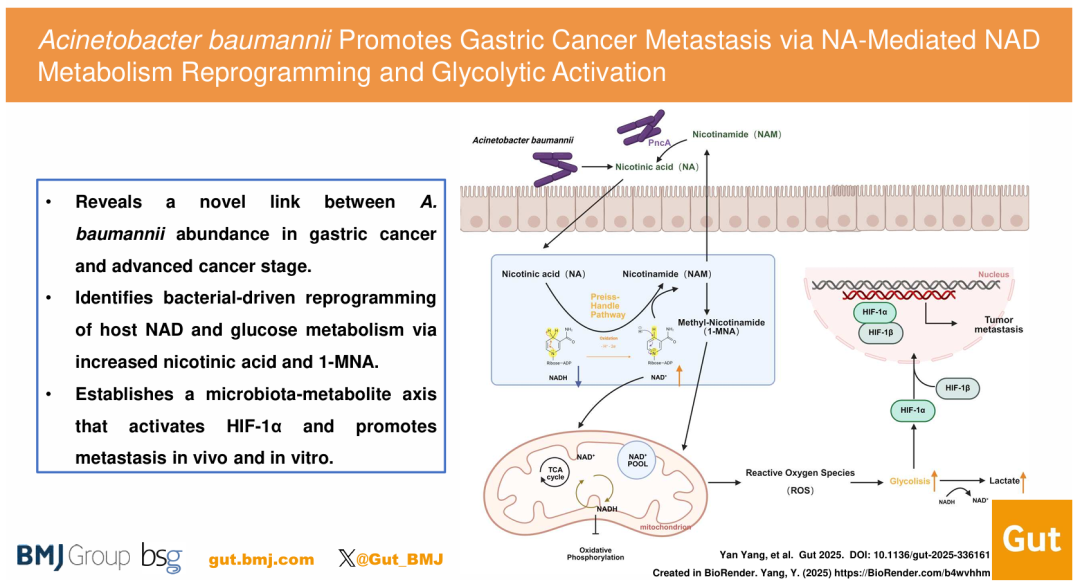
图源:GUT 机理模式图
02新药成果密集落地
ADC药物覆盖多靶点、多治疗阶段
2025-2026年是胃癌ADC药物临床转化的关键突破年,多款靶向HER2、CLDN18.2的ADC新药完成关键临床研究。
从HER2阳性胃癌二线治疗空白的填补,到CLDN18.2 ADC全球首个注册临床的完成,再到联合治疗方案的惊艳数据,ADC药物已实现多靶点、多治疗阶段、单药+联合的全面覆盖,成为胃癌精准治疗的核心力量。
(一)HER2 ADC:德曲妥珠单抗获批二线适应症,改写后线治疗格局
HER2阳性胃癌曾长期面临“一线曲妥珠单抗治疗失败后无有效靶向方案”的困境,而2026年1月,德曲妥珠单抗(T-DXd)获NMPA批准单药用于HER2阳性胃癌二线治疗,成为中国首个且唯一获批该适应症的ADC药物,填补了临床空白,其审批从递交上市申请到获批仅用时6个月,彰显了创新药的临床价值。

此次获批基于国际多中心III期DESTINY-Gastric04研究的重磅数据,该研究结果发表于《新英格兰医学杂志》,证实与传统雷莫西尤单抗联合紫杉醇方案相比,德曲妥珠单抗将患者中位总生存期(OS)从11.4个月提升至14.7个月,死亡风险降低30%,24个月OS率实现翻倍(29% vs 13.9%);中位无进展生存期(PFS)从5.6个月提升至6.7个月,客观缓解率(ORR)达44.3%。

(二)CLDN18.2 ADC:国产原研领跑全球,多药物展现优异疗效
CLDN18.2是胃癌ADC药物研发的核心赛道,2025-2026年该领域国产原研药实现全球领跑,多款药物完成关键临床研究并公布惊艳数据。
- 礼新医药LM-302:2026年2月完成全球首款CLDN18.2 ADC三线及以上治疗胃癌的III期注册临床全部受试者入组,成为该领域的里程碑事件。 这款国家1类创新药可特异性结合CLDN18.2阳性肿瘤细胞,经内吞作用释放毒素实现精准杀伤。目前其多个适应症被CDE纳入突破性疗法,还获得美国FDA孤儿药资格认定,一线联合免疫治疗的III期研究也在计划中。 来源:中国生物制药公告
- 德琪医药ATG-022:2025年ASCO GI公布的I/II期CLINCH研究数据显示,该药物在不同CLDN18.2表达水平的晚期胃癌患者中均展现出良好的疗效和可控的安全性。 来源:德琪医药公告
- 君实生物JS107:2025年ESMO GI公布的一线三联治疗I期数据惊艳业界,其联合特瑞普利单抗+XELOX化疗方案,治疗效果与CLDN18.2表达水平呈正相关,显示出显著的抗肿瘤疗效,实现了较高的缓解率和潜在生存改善,同时安全性可控。 该方案通过“ADC精准靶向+免疫激活+化疗压制”的三重机制实现协同抗癌,且安全性可控,为CLDN18.2阳性胃癌一线治疗提供了全新方案。 来源:ESMO,医学部整理汇总
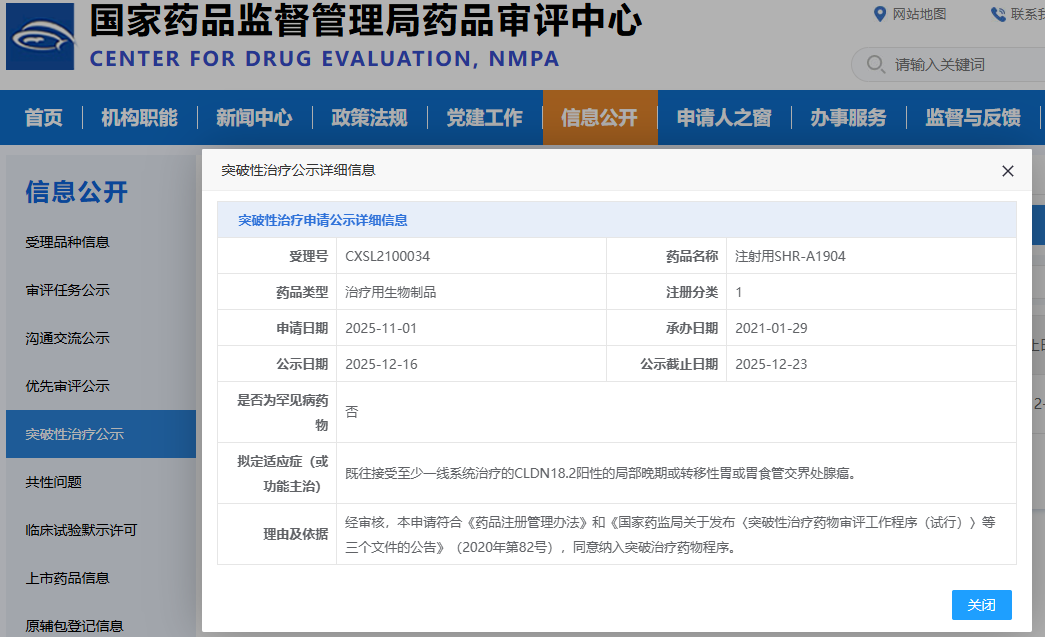
- 恒瑞医药SHR-A1904:2025年12月16日,恒瑞医药靶向CLDN18.2的ADC药物SHR-A1904被CDE纳入突破性疗法,拟定适应症为经至少一线系统治疗的CLDN18.2阳性局部晚期或转移性胃/胃食管交界处腺癌。 该药物以拓扑异构酶抑制剂为有效载荷,可通过靶向结合肿瘤细胞并内吞释放毒素实现杀伤,展现出良好的抗肿瘤活性和可控安全性,为经治患者提供新选择。
(三)联合治疗:ADC+免疫/化疗成主流,科研数据证实协同效应
基于“免疫原性细胞死亡”的基础科研结论,ADC药物与PD-1/PD-L1抑制剂、化疗的联合治疗成为胃癌治疗的核心发展方向,2025年多项临床研究证实了联合方案的协同优势,疗效较单药显著提升,为扩大获益人群、克服耐药提供了新路径。
除LM-302、JS107的联合治疗数据外,德曲妥珠单抗联合PD-1抑制剂治疗HER2阳性胃癌的研究也在积极开展,初步数据显示可有效逆转部分患者的HER2表达异质性耐药;此外,CLDN18.2双特异性抗体联合ADC药物、免疫治疗的探索也取得进展,新桥生物Givastomig联合纳武利尤单抗及化疗的Ib期数据为多靶点联合治疗提供了新思路。
这些研究证实,ADC药物与免疫治疗的联合可实现“1+1>2”的抗癌效果,成为未来胃癌治疗的主流趋势。
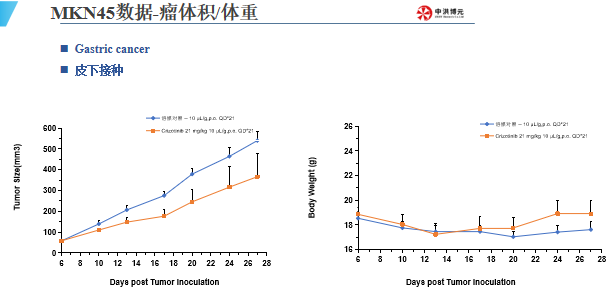
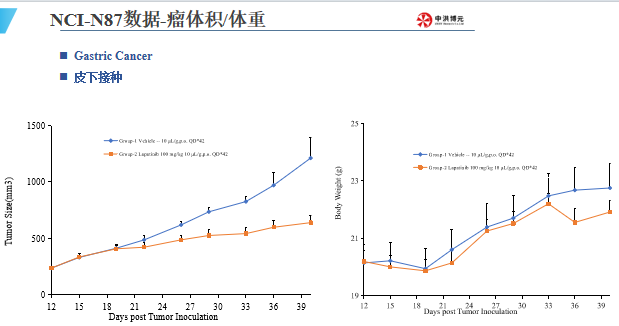
中洪博元肿瘤模型——胃癌
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
