17亿美元豪赌!安斯泰来牵手Vir,双掩蔽TCE或将改写前列腺癌治疗
2026年2月23日,日本制药巨头安斯泰来(Astellas)与Vir Biotechnology共同宣布聚焦PSMA×CD3双特异性抗体VIR-5500的研发与商业化推进。在前列腺癌治疗需求尚未被充分满足、TCE技术迭代加速的背景下,安斯泰来为何选择Vir的双掩蔽技术?

图源:雪球
此次合作呈现典型的“现金+股权+高额里程碑”模式。根据双方协议,Vir将获得总计最高17亿美元的交易额,具体条款如下:
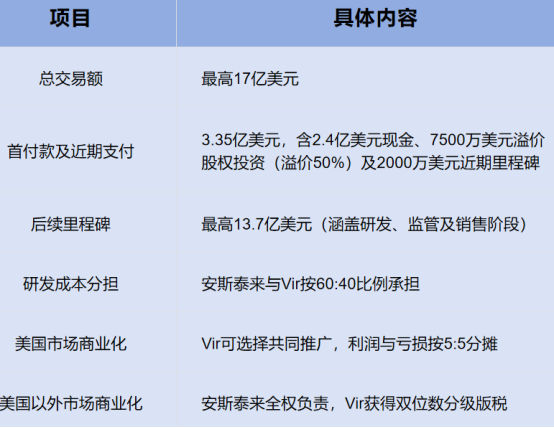
图源:凤凰涅槃之路
值得注意的是,7500万美元的溢价股权投资并非单纯的资金注入,而是安斯泰来对Vir旗下PRO-XTEN双掩蔽技术平台的公开背书——这意味着安斯泰来不仅是针对VIR-5500这一单一管线,更是对下一代TCE技术方向的认可。此外,美国市场的共推选择权为Vir保留了未来价值上行空间,而安斯泰来则凭借自身成熟的全球商业化网络,确保管线落地效率。
从交易后续市场反应来看,Vir Biotechnology股价在合作宣布后涨超38%,创下逾一年新高,而竞争对手Janux Therapeutics的股价则在近期呈现波动下行趋势,近三个月累计下跌14.19%。
安斯泰来愿意支付高额首付款在于Vir的PRO-XTEN双掩蔽平台能够精准解决当前TCE疗法的核心痛点——细胞因子释放综合征(CRS)。作为下一代免疫疗法的核心方向之一,TCE通过同时结合肿瘤细胞表面的肿瘤相关抗原(TAA)与T细胞表面的CD3受体,定向激活T细胞杀伤肿瘤细胞,但其临床应用长期受限于脱靶效应引发的CRS:一旦CD3在外周血中被过早激活,极易引发免疫风暴,进而限制药物剂量上限、压缩治疗窗口,甚至导致治疗中断。

图源:雪球
VIR-5500的差异化优势,在于其独特的“双掩蔽”结构设计:与Janux Therapeutics等竞争对手采用的单掩蔽设计(仅遮蔽PSMA端)不同,VIR-5500同时对PSMA端和CD3端进行遮蔽,使药物在进入肿瘤微环境之前保持“沉默”状态,仅在肿瘤微环境特有的酶解环境下,遮蔽肽被特异性裂解,从而激活药物活性,实现对肿瘤细胞的精准杀伤。这种设计从根源上减少了外周血中T细胞的非特异性激活,大幅降低CRS风险,同时提升肿瘤部位的药物有效浓度。
2024年8月Vir通过与赛诺菲达成独家许可协议,获得该药物及PRO-XTEN掩蔽平台的使用权利,此次与安斯泰来的合作,也将根据协议向赛诺菲分享部分合作收益。从现有I期临床数据来看,VIR-5500的安全性优势已初步显现:在58例入组患者中,50%的患者出现CRS,但均以1级(仅发烧)为主,且在未使用预防性类固醇的情况下,选定推进剂量下未出现3级及以上CRS事件;同时,12%的患者发生3级及以上治疗相关不良事件(TRAE),整体耐受性良好。
除Vir的双掩蔽设计外,天演药业、时迈药业等企业也在布局单掩蔽TCE技术,但Vir的双掩蔽设计在理论上具有更窄的脱靶效应、更宽的治疗窗口——时迈药业旗下候选药物CMDE005(单掩蔽设计)在临床前研究中,非肿瘤组织的CD3结合减少1000倍,而Vir的双掩蔽技术相关数据显示,其CD3结合抑制效果可达10000倍以上,安全性优势更为显著。这种技术差异,成为安斯泰来选择Vir的核心技术考量。
在2026年ASCO GU大会上公布的更新数据中,VIR-5500在重度经治的转移性去势抵抗性前列腺癌(mCRPC)患者中展现出强劲的疗效潜力,与Janux Therapeutics的核心候选药物JANX007形成直接竞争,具体数据对比如下:

图源:凤凰涅槃之路
从数据来看,VIR-5500与JANX007在PSA反应率上几乎旗鼓相当,但在客观缓解率上具有明显优势;更关键的是,VIR-5500的给药频率更具便利性——每3周一次的给药方案,相较于每周一次的JANX007,能够显著提升患者依从性,尤其适合前列腺癌这类慢性肿瘤的长期治疗,在真实世界应用中更具竞争力。
需要注意的是,Janux Therapeutics此前因JANX007的临床数据披露有限,曾导致股价暴跌,投资者对其数据完整性的担忧,进一步凸显了VIR-5500现有数据的可信度与竞争力。此外,与诺华已商业化的放射性配体疗法Pluvicto相比,VIR-5500若能实现门诊安全给药,将在可及性上形成显著优势。
作为安斯泰来前列腺癌业务的支柱产品,Xtandi(恩杂鲁胺)自上市以来,一直是全球前列腺癌治疗的核心药物,但该药物的专利保护期即将到期——2026年开始在部分市场失去独占地位,预计2027年前后将面临全球范围的仿制药竞争,这意味着安斯泰来亟需寻找下一代增长引擎,填补Xtandi退出后留下的市场空白。
VIR-5500的布局,不仅能够作为单药用于mCRPC患者的治疗,未来还可与安斯泰来现有雄激素通路抑制剂联合使用,形成协同治疗方案,进一步扩大治疗人群,延续其在前列腺癌领域的市场优势。
对于Vir而言,此次合作则是其从抗病毒领域向免疫肿瘤学转型的关键。Vir早期以抗病毒项目闻名,近年来逐步转向免疫肿瘤学领域,此次获得安斯泰来的溢价股权投资与深度合作,不仅为其带来充足的研发资金,更意味着大型制药企业对其PRO-XTEN双掩蔽技术平台的认可,有助于其巩固战略转型方向,提升在TCE赛道的竞争力。
前列腺癌是全球男性最常见的恶性肿瘤之一,而转移性去势抵抗性前列腺癌(mCRPC)作为疾病的终末阶段,其临床治疗仍面临巨大困境——患者5年生存率仅约30%。mCRPC治疗目前存在三大核心挑战:后线治疗选择匮乏,新型内分泌治疗耐药后,传统化疗毒副作用难以被高龄、体弱者耐受;治疗副作用与生活质量维护存在突出矛盾,现有治疗的副作用常与患者本身的骨痛、癌性乏力等症状叠加,甚至导致患者放弃治疗;缺乏精准高效的系统性治疗,无法在强效攻击肿瘤的同时规避对正常组织的损伤。
目前,除诺华的Pluvicto外,全球尚无成熟的TCE疗法用于前列腺癌治疗,而TCE疗法凭借其精准靶向、强效杀伤的优势,有望成为突破mCRPC治疗困局的重要方向。
从市场规模来看,TCE赛道正处于快速增长期,全球TCE药物市场规模在2024年达30亿美元,预计到2030年将扩大至475亿美元,复合年增长率达58.6%,到2035年全球市场规模有望突破1200亿美元。其中,实体瘤TCE是未来增长的核心动力——目前全球已获批的TCE疗法多针对血液瘤,针对实体瘤的仅2款,而前列腺癌作为实体瘤中的大适应症,其TCE市场潜力巨大,这也成为安斯泰来、诺华、安进等企业竞相布局的核心原因。
从行业发展趋势来看,PSMA赛道掩蔽型TCE成为竞争焦点,安全窗口成为产品竞争力的核心指标,大药企与生物技术公司的合作模式也日趋深度化,从单纯的管线授权转向技术平台共建、商业化共推,实现优势互补。除Vir与Janux外,艾伯维、天演药业、时迈药业等企业均在布局相关技术,其中艾伯维与Xilio Therapeutics的合作金额超21亿美元,时迈药业的CMDE005(单掩蔽TCE)已进入临床阶段。
未来胜负的关键或许不在于谁最早进入前列腺癌市场,而在于谁能够在疗效、毒性与使用便利性之间找到最优解。这场17亿美元的押注,其最终走向注定将深刻影响全球前列腺癌的治疗格局。
尽管VIR-5500目前展现出良好的疗效与安全性潜力,但其未来能否成为“best-in-class”产品,关键取决于三期临床试验的表现。根据双方规划,2026年第二季度将启动针对转移性激素敏感性前列腺癌(mHSPC)的1期剂量扩展研究,2027年计划进入3期临床试验,而双掩蔽设计能否在更大样本量中维持稳定的安全窗口,将是决定其成败的核心节点。
中洪博元前列腺癌模型数据部分展示
PC-3数据-瘤体积/体重
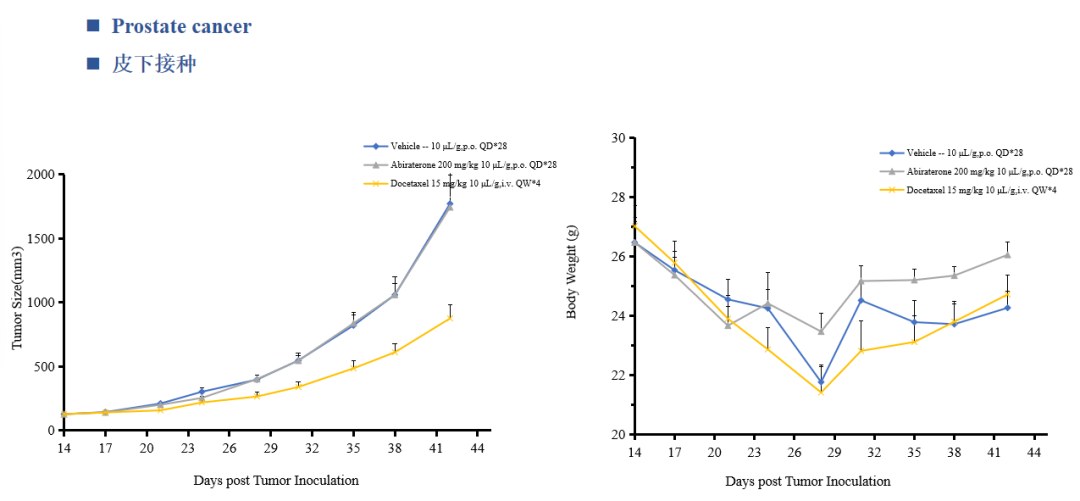
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
