每年影响全球数亿人!特应性疾病迎来机制突破与靶向治疗新纪元
随着发育免疫学、单细胞组学及双特异性抗体技术的飞速发展,特应性疾病(尤其是特应性皮炎)领域在发病机制源头革新与精准治疗策略方面取得了多项原创性成果。
近期 《Nature》、《柳叶刀》 等顶刊及国际顶级医学会议连续发表的突破性研究,结合本土药企的创新管线推进,为这类顽固的慢性炎症性疾病提供了从“被动控制”到“主动干预与预防”的全新视角。
图源:nationaleczema
特应性皮炎(Atopic Dermatitis, AD)是一种以严重瘙痒和慢性皮损为核心特征的系统性免疫性疾病,全球儿童患病率高达20%,成人患病率约5%,且常与哮喘、食物过敏等特应性共病相伴相生,形成困扰患者终身的“特应性进程”。
据《柳叶刀》相关研究数据,中重度AD患者生活质量评分甚至低于部分心血管疾病患者。长期以来,Th2型免疫应答被认为是AD发病的核心环节,但生命早期免疫印迹、细胞间代谢交互、以及难治性患者的炎症通路偏移等关键机制尚未完全阐明,临床治疗仍面临长期用药安全性及应答率有限的挑战,亟需全新路径实现突破。
生命早期免疫“检查点”:pii-DC驱动远期过敏易感性
过敏性疾病常在生命早期发生,但不同年龄阶段免疫系统对过敏原的应答机制长期缺乏系统认知。2026年2月 《Nature》 发表西奈山伊坎医学院研究,首次系统解析了生命早期对过敏原的独特应答模式,提出了 “外周免疫诱导型树突状细胞(pii-DC)” 这一颠覆性概念。

图源:nature
核心机制:研究显示,新生期皮肤暴露于过敏原会表现出一种分叉式免疫模式——局部皮肤由γδ T17细胞主导强烈的type 17炎症反应,而淋巴结内同时进行经典的Th2致敏。这种早期炎症具有短暂时间窗,但会对远期免疫结局产生持久影响:新生期暴露于过敏原的个体,在成年后二次气道暴露时,肺部Th2炎症、嗜酸粒细胞浸润及IgE反应显著增强。
细胞与分子机制:研究进一步揭示,这种早期皮肤炎症由真皮Vγ6+ γδ T细胞驱动,其无需TCR刺激即可产生IL-17A。而上游的关键启动者并非传统认知的迁移性DC,而是一种驻留于皮肤原位直接激活免疫反应的pii-DC。新生期cDC2摄取过敏原后上调Il12b等炎症基因并产生IL-23,直接激活局部γδ T17细胞。值得注意的是,这一pii状态具有明显的年龄依赖性,受神经内分泌发育调控:新生期下丘脑-垂体-肾上腺轴未成熟,低糖皮质激素水平允许DC进入pii状态;而敲除DC的糖皮质激素受体可在成年期重现该表型。
临床意义:该研究不仅揭示了早发AD的免疫基础,更提出了一个由神经内分泌发育设定的免疫检查点窗口,为靶向生命早期干预以阻断特应性进程提供了全新理论依据。
微环境交互与代谢重编程:细胞对话中的新靶点
特应性皮炎的病理网络远不止于T细胞,树突状细胞与角质形成细胞的异常对话以及脂质代谢紊乱构成了疾病进展的闭环放大通路。
WTAP-m6A-ALOX15轴:DC-角质形成细胞对话的关键介质
2026年 《Life Sciences》 发表的研究深入探讨了RNA表观修饰在AD中的作用。研究发现,AD皮损中树突状细胞的ALOX15表达显著上调,且与疾病严重程度相关。机制上,m6A甲基转移酶WTAP通过m6A修饰增强ALOX15表达,促使DC活化并分泌大量炎症因子及花生四烯酸代谢产物(LTB4、12-HETE、15-HETE)。这些代谢物进而导致角质形成细胞分化异常、增殖紊乱及脂质代谢障碍——这正是AD特征性的表型变化。该WTAP-m6A-ALOX15轴的确立,为靶向“脂质代谢重编程”和“DC-角质形成细胞对话”提供了新的干预切入点。

图源:sciencedirect
ILC2与“远程启动”:从皮肤到肠道的致病通路

图源:springer
《Clinical Reviews in Allergy & Immunology》的综述系统阐述了2型先天淋巴细胞(ILC2) 在特应性进程中的核心作用。在屏障受损的皮肤中,IL-33激活ILC2,后者不仅产生IL-5和IL-13,还通过“远程启动”机制促进肠道肥大细胞增殖及IgE类别转换,从而介导食物过敏的发生。值得注意的是,虽然外用糖皮质激素(TCS)可改善皮损,但婴儿AD患者经TCS治疗后,角质层中IL-5和IL-13仍持续升高,提示ILC2在局部持续活跃,这解释了为何单纯激素治疗难以阻断特应性进程。
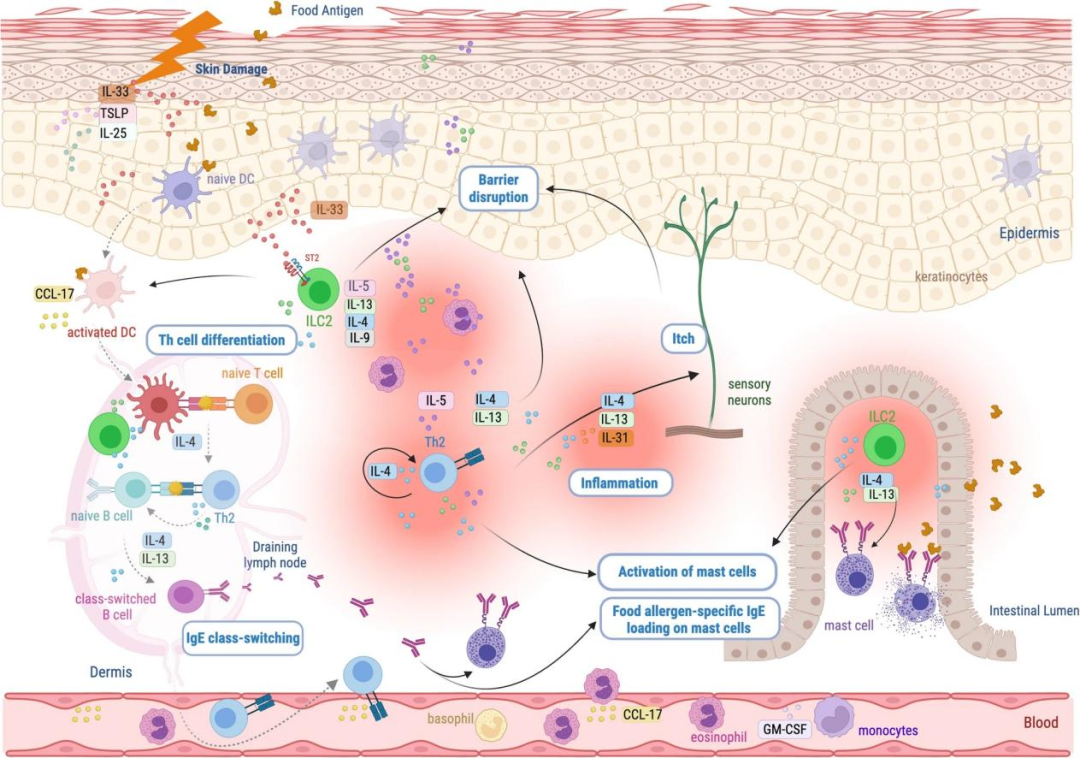
图源:springer
临床治疗转化:从靶点验证到精准干预
机制的革新直接推动了治疗策略的升级,实现了从“广谱抑制”到“精准阻断”的跨越。2025-2026年,多条核心通路迎来临床验证里程碑。
(一)OX40-OX40L通路:开启AD持久缓解新纪元
OX40信号是T细胞致病性活化与记忆形成的关键共刺激分子。2026年 《柳叶刀》 正式发表了OX40靶向单抗Rocatinlimab治疗中重度AD的关键III期临床结果(ROCKET-IGNITE 与 ROCKET-HORIZON)。

图源:lancet
· 疗效突破:在ROCKET-IGNITE研究中,300mg剂量组42%的患者实现EASI-75(皮损改善≥75%),显著高于安慰剂组的13%;vIGA-AD评分为“完全/几乎清除”的患者比例达24%。更为关键的是,疗效随时间推移持续增强,至24周研究结束时仍未达平台期,提示其具备改变疾病进程的潜力。
· 安全性:常见不良事件多为一过性注射反应,严重不良事件发生率低(2%-5%),与安慰剂组相当。
该结果不仅验证了OX40通路的临床价值,更为AD患者提供了首个有望实现长期缓解的靶向疗法。目前,国产创新药企如百奥泰(BAT6026,ADCC增强型OX40单抗)、赛诺菲(Amlitelimab,“非耗竭性”OX40配体阻断剂)及Pogee Therapeutics(超长效OX40L单抗,半衰期约60天) 均在该赛道快速推进。
(二)IL-4Rα靶向深化迭代:国产力量崛起与双特异性突破
IL-4Rα作为Th2通路的共同受体,仍是AD治疗的基石。
· 国产新药上市推进:2026年2月,康方生物的IL-4Rα单抗曼多奇单抗(AK120) 上市申请获NMPA受理。其III期临床研究在主要终点、关键次要终点上均取得统计学显著性和临床意义的双重改善,尤其在早期瘙痒改善指标上表现优异。这预示着国产IL-4Rα抑制剂即将进入商业化阶段,为患者提供更多元的经济可及选择。

图源:康方生物
· 双抗引领下一代疗法:更具突破性的是,康方生物自主研发的全球首个IL-4Rα/ST2双特异性抗体AK139,已获批开展包括中重度AD在内的7项适应症II期临床。ST2是IL-33的特异性受体,IL-33是警报素家族关键成员。AK139可同时阻断IL-4/IL-13(Th2轴)和IL-33/ST2(先天炎症轴)两条通路,早期研究显示其在抑制炎症因子释放、组织炎症浸润等指标中展现出显著优于单靶点抗体的协同效应。这标志着AD治疗正从单靶点迈向“双靶点协同”的新时代。

图源:康方生物
(三)解锁新通路:MRGPRX2与IL-18的临床验证
针对现有疗法应答不佳的患者群体,全新作用机制的药物正进入临床后期。
· MRGPRX2拮抗剂:Evommune公司的口服小分子MRGPRX2拮抗剂EVO756正在开展AD的IIb期临床(预计2026年下半年数据读出)。MRGPRX2是表达于肥大细胞和感觉神经元上的受体,可直接介导非IgE依赖的假性过敏反应和瘙痒。靶向该通路有望同时调控肥大细胞活化和神经源性炎症。
· IL-18抑制剂:Evommune的IL-18结合蛋白融合蛋白EVO301也已进入AD的II期临床(预计2026上半年数据读出)。IL-18作为炎症小体下游效应分子,在部分AD亚群中发挥驱动作用。
(四)重塑长期管理策略:从控制症状到干预进程
2026年《Clinical Reviews in Allergy & Immunology》的研究强调,对于婴幼儿AD,治疗目标应超越皮损清除,着眼于阻断特应性进程。数据显示,与TCS单药治疗相比,度普利尤单抗联合TCS治疗16周可使6个月至5岁患儿的IgE水平降低70%(TCS单药组升高30%)。这提示,早期、强效的靶向干预可能改变患儿的远期过敏轨迹。
结语与展望
当前特应性疾病研究已形成 “发育起源—细胞代谢互作—多通路网络调控” 的完整机制图谱,并快速转化为临床可及的靶向策略。从pii-DC揭示的生命早期干预窗口,到OX40靶向的持久缓解潜力,再到IL-4Rα/ST2双抗等下一代疗法的涌现,我们正见证着特应性疾病治疗从“症状控制”向 “疾病修饰与预防” 的深刻转型。
未来,随着单细胞多组学进一步筛选新型亚群特异性靶点,以及双抗、小分子口服药、外用制剂等多样化 modalities 的融合,个体化、精准化的治疗路径将愈发清晰。中国本土创新力量如康方生物、百奥泰的深度参与,也将加速这一变革,为数以亿计的特应性疾病患者带来重获健康生活的曙光。
中洪博元特应性皮炎模型
造模方法:选择健康SPF级Balb/c小鼠,实验前颈背部区域脱毛,造模时,于颈背部均匀涂布工作液,右耳内测均匀涂布,每天一次,持续数天。
阳性药物:醋酸地塞米松软膏,治疗期间维持造模。
模型数据
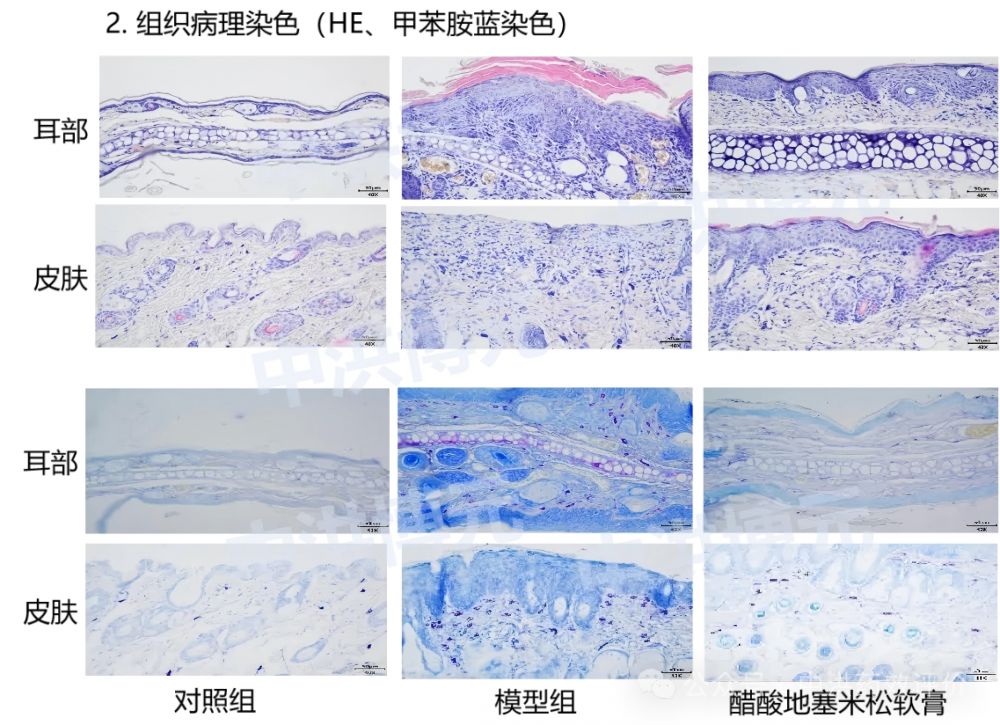
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
