嗅觉跨界,代谢破局——Or5v1/Olfr110解锁肥胖新标
肥胖从来不是多吃几口的体态小事,而是悄悄诱发糖尿病、脂肪肝、心血管疾病乃至多种癌症的“隐形杀手”。2026年1月21日,山东大学孙金鹏教授团队联合多所高校及医院团队在Cell发表重磅研究Identification of Or5v1/Olfr110 as an oxylipin receptor and anti-obesity target,这是一场“跨界逆袭”:嗅觉受体Or5v1/Olfr110,这个原本只负责“闻香辨味”的专职选手,居然藏着抗肥胖的隐藏技能,被证实是全新抗肥胖靶点。

图源:Cell
长久以来,肥胖治疗是“内卷重灾区”,始终陷在靶点撞脸、疗效拉胯。减重代谢手术创伤大、恢复慢,人望而却步;GLP-1RA类药物虽火,却逃不过“吃了吐、停了胖”的魔咒,胃肠道不良反应让人半途而废。
这场突破的起点,源于一个长期悬而未决的科学难题:氧化脂质12(S)-HEPE早已被证实能改善葡萄糖代谢、减少脂肪堆积,它由鱼油中的EPA经酶促氧化生成,是天然的“代谢调节因子”,但介导其作用的特异性受体却始终未知。与此同时,嗅觉受体因普遍对配体亲和力低、功能被认定为“仅负责嗅觉感知”,长期被排除在氧化脂质受体的研究之外。
研究团队自主开发“反向G蛋白下拉法介导的未知受体鉴定技术”(ARIG)。传统受体筛选是大海捞针,而ARIG技术给12(S)-HEPE通过标记G蛋白亚基重构配体-受体复合物,再结合质谱分析,精准找到“灵魂伴侣”——Olfr110(人类同源体OR5V1)。解决了“受体鉴定”的核心难题,为肥胖靶点研发打开了一扇新世界大门。
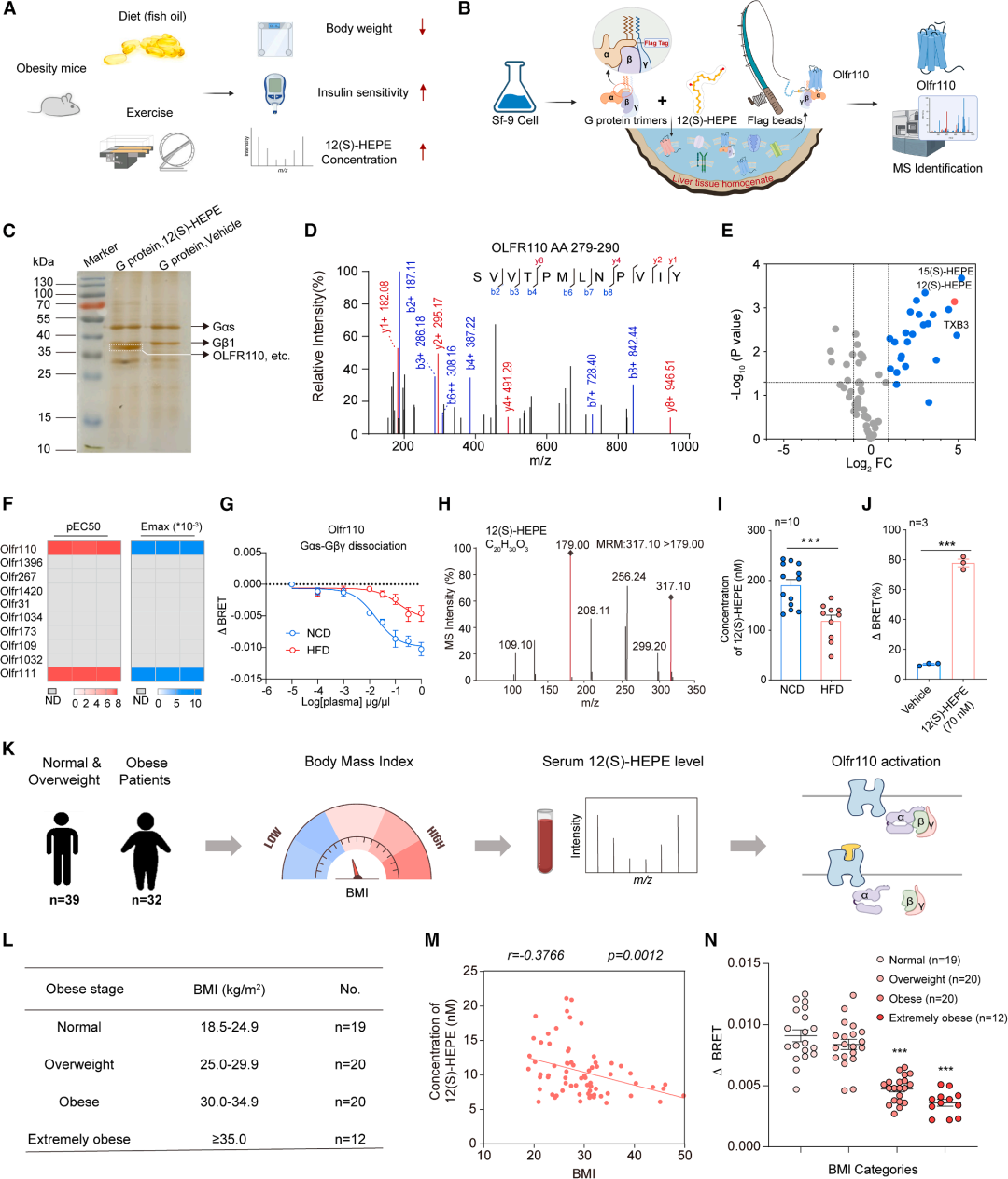
图源:Cell 图2. 鱼油饮食或运动后血浆12(S)-HEPE水平升高能够激活Or5v1/Olfr110
在HEK293细胞实验中,12(S)-HEPE激活Olfr110的EC50仅为16.0±1.1nM,而人类血清中12(S)-HEPE的浓度恰好卡在5.9~21.1nM的黄金区间,还和BMI成了死对头——肥胖人群血清激活Olfr110的能力,比正常人群弱了一大截,相当于受体“罢工”,体重自然“失控”。随后的基因编辑小鼠实验,更是直接锁定了Olfr110的“办公地点”:肝脏就是它调控代谢的“核心工作站”。把肝脏里的Olfr110“请走”,小鼠不管吃正常粮还是高脂粮,都会变成“小胖子”,代谢也一塌糊涂;而重新给肝脏“请回”Olfr110,小鼠又能恢复“苗条身材”,这一发现也为后续精准用药、避免“误伤”其他器官提供关键依据。

图源:Cell 图4. 分子机制探索
12(S)-HEPE-Olfr110-Gs-PKA-pATF2-Cpt1α的调控通路:12(S)-HEPE与Olfr110结合后,激活Gs蛋白触发信号级联反应,最终上调脂肪酸氧化关键酶Cpt1α的表达,加速肝脏脂肪分解,实现葡萄糖稳态改善。解释了12(S)-HEPE的代谢调节作用。
基于Olfr110的晶体结构,团队通过AI筛选百万级化合物库,成功开发出高选择性激动剂HOR1-C59——其对Olfr110的EC50达7.12±1.57nM,且不会激活其他同源嗅觉受体,特异性极强。在高脂饮食诱导的肥胖小鼠中,HOR1-C59能显著抑制体重增长、提升能量消耗,改善葡萄糖耐受与肝脏脂肪变性,且这一效应在Olfr110敲除小鼠中完全消失,证实其作用严格依赖目标靶点,为口服抗肥胖药物提供了优质候选分子。这种“靶点精准、通路清晰、药物可控”的研发思路是当前肥胖治疗领域最需要的创新。
当前,肥胖治疗领域的“顶流”还是GLP-1RA类药物,它短期减重效果确实“能打”,但短板也很明显:胃肠道不良反应找上门,不少人吃了就恶心、呕吐,而且部分患者停药1年后,体重会“反弹报复”,白忙活。为了弥补这个遗憾,融合诺奖理论的“新一代GLP-1RA”应运而生,试图通过“延长信号传导”扳回一局。但不管是老款还是新款,本质上都是“全身撒网”,难免“误伤友军”,出现全身副作用。而Or5v1/Olfr110的“肝脏专属属性”,精准狙击脂肪,不打扰其他器官,既能搞定代谢问题,又能降低副作用,和GLP-1RA形成鲜明对比。
除了Or5v1/Olfr110这一“嗅觉跨界”靶点,当前其他研究者还在探索靶向黑皮质素4受体(MC4R)、酰基辅酶A合成酶5(ACSL5)等新型靶点,试图通过多靶点协同调控,实现“减重不减肌肉、避免反弹”的健康目标。药明康德、中洪博元等机构也在同步推进临床前模型创新,开发表达人类GIP受体的肥胖小鼠模型,解决多靶点药物临床前评价的精准度问题,为创新药物研发提供支撑。
研究证实,补充鱼油或坚持运动,能提升体内12(S)-HEPE水平,进而激活Olfr110改善代谢——这一发现将“天然干预”与“精准用药”有机结合,符合当前行业综合防控发展方向。随着我国健康体重管理门诊的普及,这种“机制明确、可落地”的综合方案,有望成为未来肥胖防控的主流模式。
当然,金无足赤,这项研究也有小遗憾:Olfr110在肝脏里具体驻扎在哪些细胞、融合蛋白标记会不会影响它的工作位置,还有HOR1-C59长期使用会不会有后遗症,这些都还需要后续慢慢探索。
Or5v1/Olfr110靶点优势在于,其肝脏特异性表达降低了副作用风险,HOR1-C59的高选择性避免了脱靶效应,而清晰的代谢调控通路则为后续药物优化提供了明确方向。若能顺利完成临床转化,这款候选药物有望弥补当前GLP-1RA类药物的短板。
跨界创新往往能绝处逢生。嗅觉受体家族就像一个宝藏库,还有很多成员没被挖掘,这为肥胖及代谢疾病研发留下了巨大探索空间。未来,随着更多精准靶点的挖掘、创新药物的临床转化,以及综合防控体系的完善,“健康减重、精准控重”将不再是难题,而中国研发也将持续引领全球肥胖治疗领域的发展方向。
中洪博元肥胖症模型介绍——小鼠肥胖症模型
肥胖症是一种由多种因素引起的慢性代谢性疾病,表现为体内脂肪堆积过多和(或)脂肪分布异常,通常伴有体重增加。
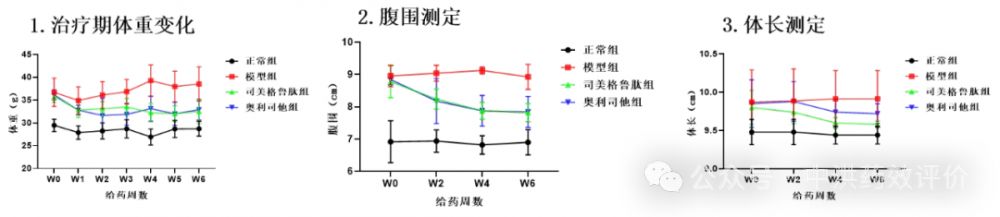
造模:5周龄BALB/c 雄性小鼠适应性饲养1周,正常组给予普通饲料喂养 14 周,自由饮水。模型组给予高脂饲料喂养 14 周,自由饮水。
造模周期:14周
阳性药物:司美格鲁肽注射液;奥利司他胶囊

免责声明:本文内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
