阻击阿尔茨海默:年增千万患者之下,早筛与靶向降解带来全新生机
阿尔茨海默病(Alzheimer‘s disease, AD)作为最常见的神经退行性疾病,已成为全球公共卫生领域最为严峻的挑战之一。据《柳叶刀》神经病学委员会最新数据显示,全球痴呆症患病人数已超过5700万,其中AD是主要病因,且预计到2050年这一数字将激增。

长期以来,AD药物研发深陷“高失败率”泥潭,针对淀粉样蛋白(Aβ)的传统策略虽能清除斑块,却常伴随脑水肿和出血(ARIA)等严重副作用,且临床认知获益有限。然而,随着2025-2026年间单细胞多组学、蛋白降解靶向技术(TPD)及超灵敏血液生物标志物的爆发式突破,AD研究正经历从“单一清除病理蛋白”向“精准调控细胞微环境”的范式转移。本文将从新机制解析、新技术颠覆、新靶点转化三个维度,描绘这一领域的革命性进展。
突触囊泡蛋白SV2A:连接突触功能障碍与Aβ生成的上游新机制
长期以来,Aβ的沉积被认为是AD级联反应的始动因素,但触发APP淀粉样蛋白酶切的上游事件仍成谜。传统观点认为,突触囊泡蛋白2A(SV2A)仅参与突触囊泡循环,且其在AD早期脑内的显著下降被视为单纯的突触丢失标志物。然而,2026年1月首都医科大学宣武医院王培昌团队在《Aging Cell》发表的研究彻底颠覆了这一认知。

图源:Aging Cell
该研究首次鉴定SV2A为一种新型APP结合蛋白。通过体内外实验证实,SV2A过表达能显著抑制APP与β分泌酶(BACE1)在内体-溶酶体网络中的异常结合,从而重塑APP的亚细胞分布,将其从淀粉样蛋白生成途径“拉回”至细胞膜表面的非淀粉样代谢途径。在APP/PS1转基因小鼠模型中,上调SV2A可使脑内Aβ斑块沉积显著减少,且这一效应独立于其经典的突触功能。

图源:Aging Cell
临床意义:这一发现不仅将AD的两大核心病理特征——突触功能障碍与Aβ沉积——通过SV2A直接联系起来,更提示SV2A可能是位于Aβ生成上游的早期干预新靶点。目前,针对SV2A的PET示踪剂已用于突触密度成像,而该研究为其向治疗性靶点的转化奠定了理论基础。
微环境与细胞交互:少突胶质细胞与Tau蛋白的“表观遗传对话”
AD的病理进展不仅是神经元的内在病变,更是由多种细胞类型参与的复杂交互网络。2026年3月《Nature Communications》发表的一项重磅研究,通过对472例AD死后脑组织进行表观基因组-wide关联分析(EWAS),揭示了以往被忽视的少突胶质细胞在Tau病理传播中的关键作用。

图源:nature
研究团队采用创新的区域甲基化(rCpGm)分析方法发现,超过99.7%的显著表观遗传变异与Tau蛋白的生化状态(特别是膜结合及不可溶形式的Tau)相关,而非Aβ。这些变异显著富集于少突胶质细胞和髓鞘形成相关基因,包括已知的AD风险基因BIN1,以及髓鞘碱性蛋白(MBP)和髓鞘相关糖蛋白(MAG)。在Tau病理负荷增高的情况下,这些区域的DNA甲基化发生显著改变,导致髓鞘相关基因表达失调,进而可能破坏神经元-胶质细胞的代谢偶联,加剧轴突损伤。

图源:nature
临床意义:该研究首次在大型队列中绘制了AD脑内的多组学表观遗传图谱,证明Tau蛋白是通过影响胶质细胞表观遗传学来驱动疾病进展的。这提示未来的治疗策略不仅要保护神经元,还需靶向保护髓鞘和少突胶细胞功能,为Tauopathies(Tau蛋白病)提供了全新的治疗窗口。
血管-免疫互作:LRP1与“外周-中枢”协同清除策略
肝脏纤维化的研究中强调了血管微循环紊乱的核心驱动作用,而在AD领域,血脑屏障(BBB)功能障碍同样被推至聚光灯下。2026年3月,中国科学院动物研究所李伟、胡宝洋团队联合国科大医学院在《Cell》杂志发表的突破性成果,巧妙利用BBB上的低密度脂蛋白受体相关蛋白1(LRP1),开发出了一种名为SPYTAC(可编程合成多肽靶向嵌合体)的新型蛋白降解技术。

图源:cell
SPYTAC技术颠覆了传统抗体药物的Fc段效应。它是一种全合成的双特异性短肽:一端结合Aβ,另一端结合LRP1。利用LRP1兼具介导跨细胞转运和引导溶酶体降解的双重天然属性,SPYTAC不仅能“挟持”外周血中的Aβ进入细胞降解,还能像“特洛伊木马”一样携带药物穿越BBB,进入大脑清除Aβ斑块。在5xFAD小鼠模型中,SPYTAC不仅有效降低了血浆和脑组织中的Aβ负荷,显著改善认知功能,更重要的是,由于其不含Fc片段,完全避免了小胶质细胞过度活化及随之而来的ARIA并发症(如微出血),展示了优于单抗的安全性。
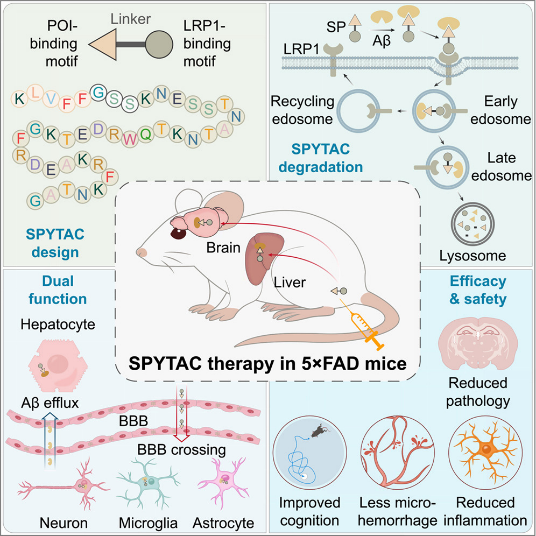
图源:cell
临床意义:SPYTAC是首个实现外周与中枢Aβ协同清除的模块化平台。它不仅为AD提供了更安全的疗法,其可编程特性(替换靶向肽)也为Tau、α-突触核蛋白等其他致病蛋白的清除开辟了通用型技术路径。
临床治疗转化:从“症状修饰”迈向“精准预防”与“精神症状干预”
机制的革新直接推动了临床管线的爆发,AD治疗已不再局限于延缓认知 decline,而是向超早期干预和精神行为症状两大蓝海迈进。
(一) 血液多组学预警:提前15年锁定风险人群
早期干预的前提是精准识别“临床前AD”患者。2026年1月《JAMA Network Open》发表的一项里程碑研究,对近300名主观认知下降(SCD)人群进行了长达15年的随访。结果证实,利用Quanterix的Simoa超灵敏技术联合检测四项核心生物轴指标——Aβ42/40比值(淀粉样蛋白)、p-Tau217(Tau病理)、GFAP(神经炎症)和NfL(神经退行性变),能极其精准地预测认知进展风险(C-index达0.90)。单一时间点的多因子组合检测,其预后价值远超单独的p-Tau217检测。

图源:JAMA Network Open
转化应用:这标志着AD筛查进入“多组学风险评分”时代。目前,基于该组合的LucentAD Complete测试已投入应用,为临床试验筛选“快速进展者”及临床前预防提供了强有力的工具。
(二) 精神症状干预:M4受体偏向激动剂的临床突破
约50%的中重度AD患者会出现激越(Agitation)等神经精神症状,但目前缺乏安全有效的疗法。2026年1月,纽欧申医药(NeuShen Therapeutics)宣布其高选择性M4毒蕈碱乙酰胆碱受体正向变构调节剂(PAM)NS-136,获得FDA批准直接进入针对“阿尔茨海默病激越(AAD)”的II期临床研究。NS-136通过调节皮质下多巴胺能系统失衡来改善激越症状,同时在临床前展现了避免非选择性胆碱能副作用的潜力。

图源:neushen
(三) 下一代Tau疗法与突触保护
尽管部分Tau抗体临床遇挫,但靶向特定翻译后修饰的精准Tau疗法仍在推进。同时,Cognition Therapeutics公司的口服小分子CT1812正在开展针对路易体痴呆(DLB)的IIb期临床,其机制在于通过作用于sigma-2受体,阻断Aβ和α-突触核蛋白对突触的毒性攻击,展现了“突触保护”这一不依赖于直接清除蛋白aggregates的差异化策略。

图源:ir.cogrx
随着SPYTAC等平台技术的验证和血液多组学的普及,我们正站在从“延缓疾病”到“预防认知功能丧失”的拐点之上。未来,随着更多像NS-136这样针对非认知症状的疗法落地,AD的精准整合治疗时代已然来临。
中洪博元阿尔茨海默症模型
造模方式:转基因小鼠继续饲养4周后进行巴恩斯迷宫和旷场实验行为学检测,检测后进行脑组织的病理检测以及Aβ42和NEP的表达情况。
造模周期:4周
阳性药:盐酸美金刚片
模型数据
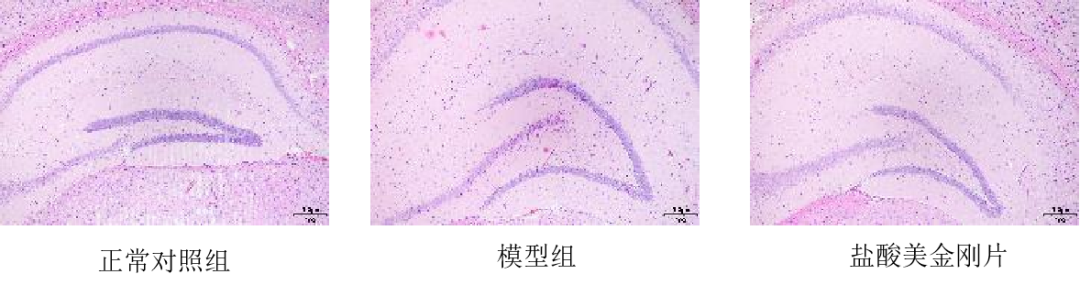
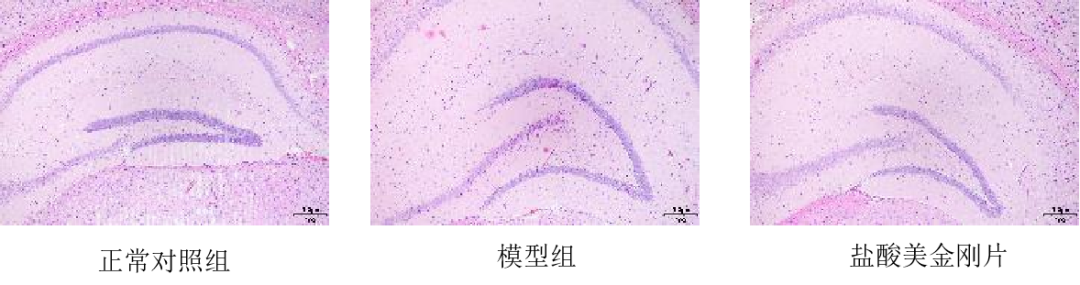
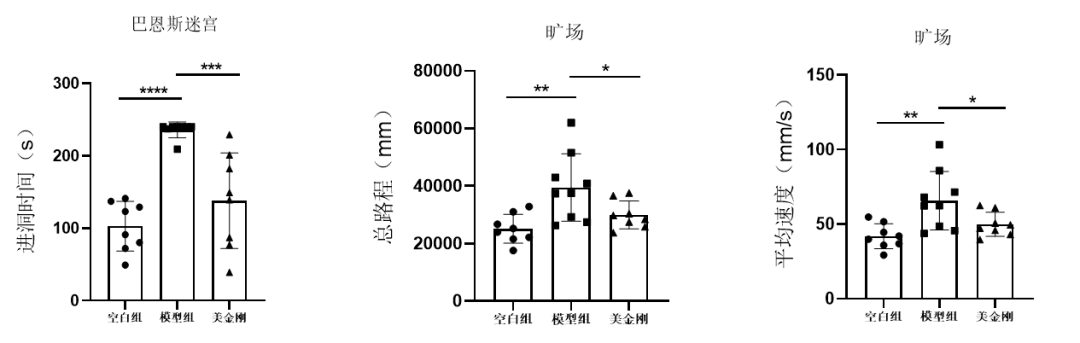
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
