从成药性到临床:肝癌药效研发新突破
肝癌作为全球第三大致死性癌症,我国发病与死亡负荷均占全球近半数,且超70%患者初诊为中晚期,临床治疗长期受限于现有疗法药效不足、毒性显著、响应率低等瓶颈。近期,我国在肝癌基础研究、临床方案及药物转化领域均有突破。
突破一
深圳湾实验室冯根生团队发表研究Advancing liver cancer immunotherapy beyond checkpoint blockade,通过递送技术优化,解决免疫调节剂polyIC的成药性难题,为药效领域“靶点/药物优化+递送系统协同”研发思路提供范例,其核心亮点:

图源: Science China Life Sciences
痛点锚定:现有肝癌免疫治疗依赖免疫检查点抑制剂,存在药效响应率低(一线联合疗法客观缓解率不足50%)、脱靶毒性显著(干扰免疫系统稳态引发肝功能障碍等不良反应)的核心问题;有效免疫调节剂polyIC因系统性毒性强、体内清除快,无法实现临床转化,其局限在于“局部浓度不足、全身暴露过高”,这也是研发免疫调节剂类药物的共性难题。

冯根生课题组
研发创新:摒弃“单纯优化靶点活性”思路,采用“药物递送+药效机制”双优化策略——将polyIC封装于脂质纳米颗粒(polyIC-LNP),通过肝靶向修饰实现精准递送,显著提升肝脏局部药物浓度,同时降低全身暴露量,从根源上解决系统性毒性问题;机制层面,通过重编程肝脏免疫微环境,诱导持久I型干扰素信号、扩增CD8 T细胞,构建异于传统检查点阻断的全新药效通路,摆脱对免疫检查点抑制剂的依赖,为非传统靶点药效挖掘提供了新方向。
药效验证:在小鼠原发及转移性肝癌模型中完成药效验证,明确低剂量单药即可实现强效抑瘤效果;同时重点验证药效的“病因非依赖性”,覆盖乙肝、酒精性肝病等不同病因肝癌模型,为后续临床药效评价及适应症拓展奠定基础,其临床前药效评价思路(聚焦局部药效、毒性控制、病因适配性)可直接借鉴于同类免疫调节剂的研发,目前该方案正推进临床转化。
突破二
东南大学附属中大医院滕皋军院士团队历经近20年攻坚,打造的肝癌“TACE介入+靶免”联合治疗方案,建立“局部治疗+系统治疗”的协同药效评价体系,为联合用药研发、药效终点设定提供重要参考,其核心亮点:

滕皋军院士
协同药效研发:针对单一TACE介入治疗药效局限(中期肝癌客观缓解率仅约30%)、单一靶免治疗适用人群窄的痛点,创新性提出“局部栓塞+免疫激活+血管抑制”的协同药效思路——TACE通过栓塞肿瘤血管造成缺血性坏死,同时释放肿瘤抗原激活免疫系统,为靶免药物发挥药效奠定基础;靶免药物则通过解除免疫抑制、抑制血管生成,放大TACE的局部抑瘤药效,形成“1+1>2”的协同效应,为联合用药的靶点搭配、给药时序优化提供借鉴。
临床药效评价体系:依托中国肝癌临床研究联盟(CHANCE)平台,构建国际最大规模的介入联合靶免治疗数据队列,通过CHANCE2005/CARES-005、TALENTACE等系列分层临床研究,明确不同分期肝癌患者的协同药效差异——中期肝癌患者采用TACE联合靶免治疗,总生存期较单纯TACE延长9.9个月;晚期患者采用该方案,总生存期较单纯靶向治疗延长6.7个月;TALENTACE研究进一步证实,“T+A”免疫靶向组合联合按需TACE,可使不可切除肝癌患者中位PFS延长至11.3个月,客观缓解率提升至81.3%。
突破三
中国生物制药“安罗替尼+派安普利单抗”(双安组合)获批晚期肝细胞癌一线治疗适应症,其Ⅲ期临床研究(APOLLO研究)成果发表于《柳叶刀肿瘤学》,是全球第二项“小分子TKI+免疫治疗”在晚期肝癌一线治疗中实现PFS和OS双终点阳性的关键研究。

图源:sinobiopharm
其立足肝癌“免疫微环境异常+血管生成旺盛”的核心病理特征,精准设计“免疫激活+血管抑制”协同药效机制——派安普利单抗(PD-1抑制剂)解除T细胞免疫抑制,激活机体抗肿瘤免疫应答;安罗替尼(小分子TKI)抑制VEGF通路,阻断肿瘤血管生成,同时改善肿瘤免疫微环境,增强免疫细胞浸润,实现协同增效,贴合“靶点互补、机制协同”的联合用药研发原则,避免同类靶点联用导致的药效叠加不足、毒性增加等问题。
该Ⅲ期临床研究,纳入649例晚期肝癌患者,其中40.9%伴有大血管侵犯,49.2%的患者甲胎蛋白(AFP)≥400ng/mL,覆盖高危人群;研究结果显示,试验组中位PFS达6.9个月(对照组2.8个月),疾病进展风险降低48%,中位OS达16.5个月(对照组13.2个月),死亡风险降低31%,双终点均达优效标准,亚组分析进一步证实高危患者获益更显著。
安罗替尼与派安普利单抗均为国产原研药物,其研发过程中注重药效与成本的平衡,目前两款药物已有多个适应症纳入国家医保目录,大幅提升临床可及性。此外,中国生物制药同步推进安罗替尼联合贝莫苏拜单抗的“得福组合”研发,拓展适应症范围,其“一款核心药物+多靶点药物联合”的研发模式,可有效提升药效覆盖范围,降低研发成本,值得借鉴。
若立足我国肝癌以乙肝相关为主的病因特征,开展精准药效验证,可提高创新药临床适配性。肝癌具有高度异质性,单一靶点与单药疗效有限,建议将联合协同作为药物研发的核心方向,重点围绕 “局部+系统”、“免疫+抗血管”、“器械+药物” 等模式,深入研究协同机制、优化给药时序、科学设定疗效评价终点。临床前药效评价构建覆盖不同病因、不同分期的标准化肝癌模型,重点关注局部疗效、安全性及药效持久性,为临床转化提供可靠依据。在创新药研发中兼顾成药性与患者可及性,持续拓展药效边界。
中洪博元肝癌模型
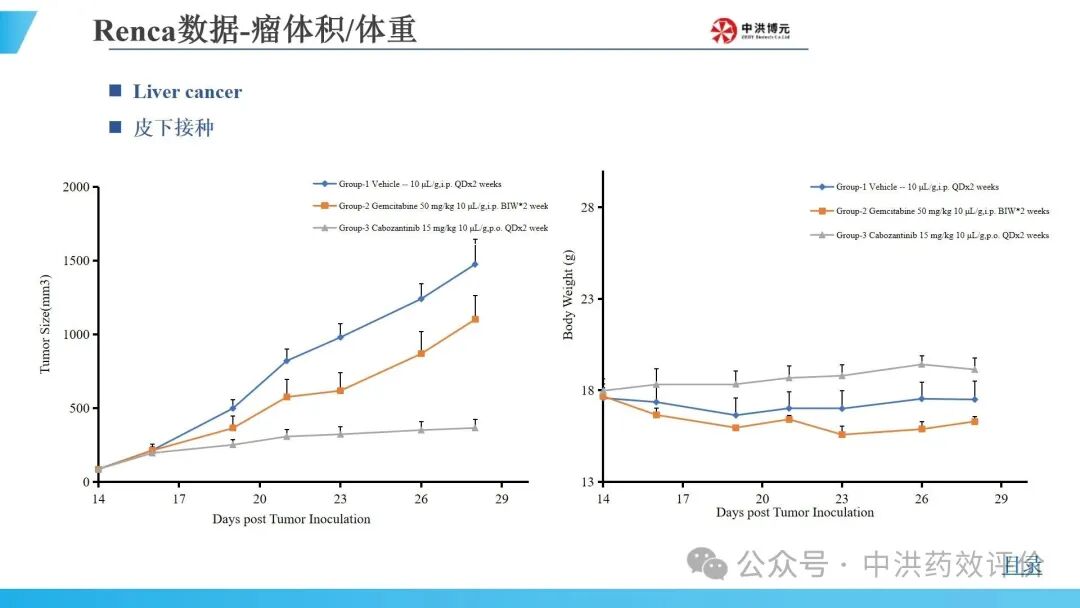

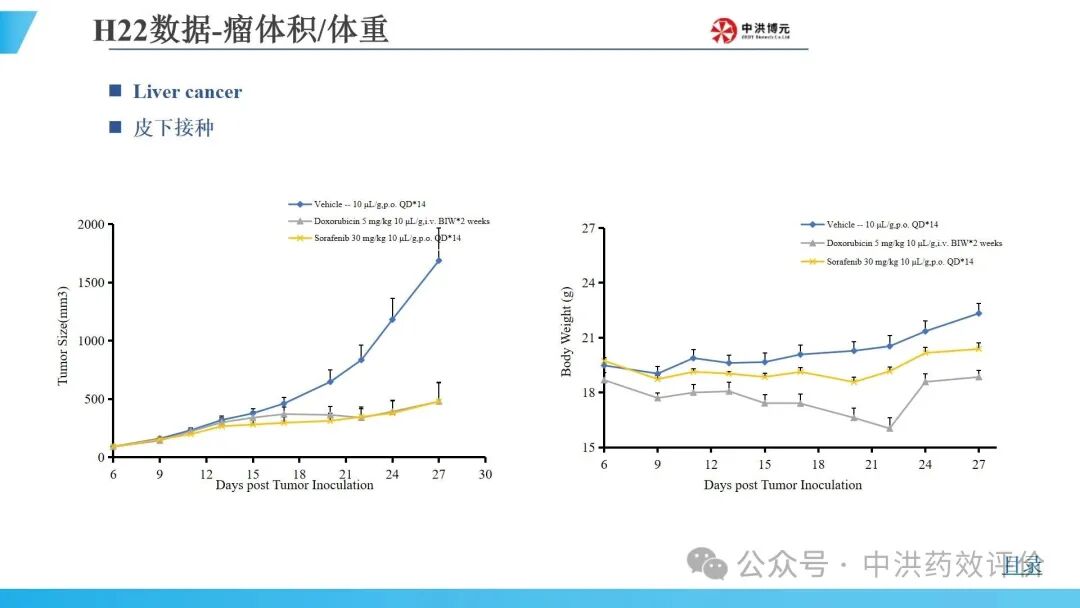

免责声明:本文内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
