胶质瘤治疗破局:从“颅内黑箱”到精准打击,多路径突破改写患者命运
胶质母细胞瘤(GBM)是最常见且最具侵袭性的原发性脑肿瘤,患者中位生存期仅12-21个月,5年生存率不足5%。长期以来,血脑屏障阻挡药物渗透、肿瘤高度异质性及免疫抑制微环境,使胶质瘤成为最难攻克的“颅内堡垒”。然而,随着溶瘤病毒、靶向药物、基因治疗及物理开放血脑屏障等技术的快速发展,胶质瘤治疗正迎来从“被动抵抗”到“主动破局”的历史性转折。

图源:sohu
机制突破:破解胶质瘤的“自筑高墙”与免疫逃逸
胶质瘤的治疗抵抗不仅源于血脑屏障的物理阻隔,更来自肿瘤自身构筑的复杂防御体系。2025年,复旦大学附属华山医院周良辅院士、史之峰教授团队在《Neuro-Oncology》发表重磅研究,首次揭示了胶质瘤在溶瘤病毒治疗压力下的“肿瘤隔离带(Tumor Self-Rampart)”抵抗机制。
图源:Neuro-Oncology
研究团队通过建立创新的RESCUE转化研究框架,利用患者来源异种移植(PDX)模型“复刻”临床治疗过程,发现溶瘤腺病毒感染肿瘤细胞后,会激活BCL10基因,进而通过NF-κB信号通路诱导细胞因子IL-8的旁分泌。IL-8进一步诱导临近未感染病毒肿瘤细胞提前进入衰老状态,这些衰老细胞在坏死区域周边聚集,形成高度纤维化的物理屏障,同时衰老细胞的病毒复制能力显著下降,构成生物屏障。这种双重屏障极大阻断了病毒在胶质瘤组织中的扩散,导致溶瘤病毒疗法“后继乏力”。
通过全基因组CRISPR筛选与空间转录组学解析,研究团队精准锁定了IL-8这一核心靶点,并筛选出IL-8受体靶向抑制剂Raperixin。与溶瘤病毒联用可有效抑制隔离带形成,显著增敏病毒复制效力。更令人意外的是,研究发现在给药早期使用糖皮质激素不仅不会因免疫抑制影响疗效,反而能通过抗炎作用消除IL-8驱动的隔离带形成,为临床精准用药提供了重要指导。
与此同时,肿瘤相关巨噬细胞(TAMs)在胶质瘤免疫逃逸中的作用也被深度解析。TAMs占胶质瘤肿瘤总量的30%-50%,其M2型极化亚群通过分泌TGF-β、IL-10等免疫抑制因子,并上调PD-L1表达,形成强效免疫抑制屏障。2025年《Frontiers in Cell and Developmental Biology》综述系统总结了TAMs介导化疗耐药的五大机制:药物代谢酶调控、促瘤因子分泌、胶质瘤干细胞互作维持干性、缺氧微环境适应、以及通过基质金属蛋白酶(MMPs)重塑细胞外基质增加组织硬度,阻碍药物渗透。这些发现为靶向TAMs的治疗策略奠定了理论基础。
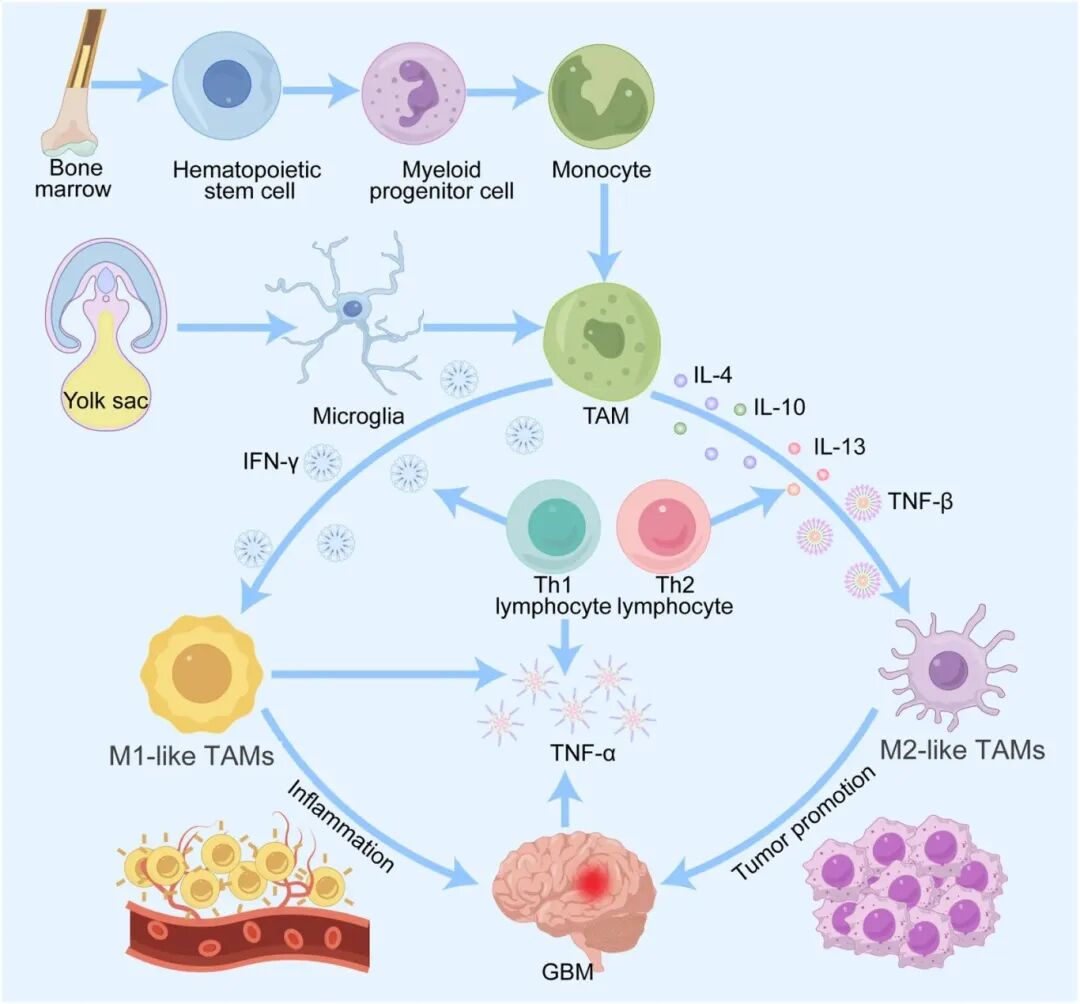
图源:frontiers
治疗策略革新:从“被动防御”到“主动破局”
(一)物理破障:聚焦超声打开血脑屏障
血脑屏障是胶质瘤药物递送的核心障碍。2025年《柳叶刀·肿瘤学》发表的BT008NA多中心I/II期试验,首次在人体中证实了微泡增强经颅聚焦超声(MB-FUS)联合替莫唑胺治疗高级别胶质瘤的安全性与可行性。

图源:ncbi
研究纳入34例新诊断高级别胶质瘤患者,在6个周期的替莫唑胺化疗期间,于每个周期前3天内进行MB-FUS治疗,精准开启肿瘤浸润区域的血脑屏障。结果显示,所有治疗均实现血脑屏障开放,无治疗相关死亡事件发生。患者中位总生存期达31.3个月,中位无进展生存期13.5个月,较历史数据显著延长。更令人振奋的是,MB-FUS治疗后血浆游离DNA水平变化与患者病程高度一致,提示该技术还可用于“声学液体活检”,实现无创动态监测。这项技术为化疗药物及后续免疫治疗进入颅内提供了物理通道,具有广泛的联合应用前景。
(二)精准靶向:IDH1突变抑制剂的里程碑突破
IDH1突变是低级别胶质瘤及部分高级别胶质瘤的关键驱动基因。2026年2月,Nuvation Bio公司宣布其口服、高效脑渗透性突变型IDH1抑制剂Safusidenib的全球III期SIGMA试验(G203)正式启动,标志着该靶点向临床转化迈出决定性一步。

图源:Nuvation Bio
Safusidenib在I/II期临床中已展现出良好的耐受性和抗肿瘤活性。此次III期试验将纳入约300例IDH1突变型星形细胞瘤患者(包括2级高危、3级及4级),主要终点为盲态独立中央评审的无进展生存期(PFS)。同时,试验还增设了约40例3级少突胶质细胞瘤患者的探索性队列,评估其在未接受放化疗患者中的客观缓解率。美国国家脑肿瘤学会总裁David Arons指出:“IDH1突变胶质瘤患者长期缺乏经证实的延长生存方案,这项注册性试验有望为这一高度未满足需求的领域带来突破。“
(三)免疫双抗+DNA药物:协同激活抗肿瘤免疫
2026年3月,康方生物与INOVIO公司达成合作协议,将共同探索全球首创PD-1/CTLA-4双特异性抗体卡度尼利联合DNA药物INO-5412治疗胶质母细胞瘤的创新方案。该联合疗法已纳入由Dana Farber癌症研究所发起的INSIGhT II期适应性平台试验。

图源:akesobio
INO-5412编码了hTERT、WT1和PSMA三种高优先级肿瘤抗原,同时编码IL-12激活T细胞免疫应答。此前II期研究显示,INO-5412联合PD-1抑制剂可诱导强劲的抗原特异性T细胞应答,并促进T细胞浸润至肿瘤微环境。卡度尼利作为全球首个获批的PD-1/CTLA-4双抗,可同时阻断两个免疫检查点,理论上可产生协同增效。Dana Farber神经肿瘤中心主任David Reardon表示:“胶质母细胞瘤是目前有效手段最为匮乏的恶性肿瘤之一,这项创新免疫联合疗法有望攻克单一检查点抑制剂难以解决的问题。”
(四)基因治疗破冰:AAV载体首获FDA IND批准
2026年2月,Siren Biotechnology公司宣布其AAV-based免疫基因疗法SRN-101获得FDA新药临床试验(IND)批准,用于治疗复发高级别胶质瘤。这是FDA首次批准AAV载体用于肿瘤适应症,标志着基因治疗在实体瘤领域的重大突破。
图源:hillgene
SRN-101采用重组AAV载体,将工程化免疫调节基因直接递送至肿瘤微环境,旨在激发持久的抗肿瘤免疫应答。临床前研究显示该疗法在脑癌模型中具有强效抗肿瘤活性。这一IND获批为基因治疗在脑肿瘤领域的应用开辟了先河,也为后续联合治疗提供了全新平台。
(五)靶向微环境:从巨噬细胞到氧化应激
针对肿瘤微环境的干预策略也在快速推进。靶向TAMs的多种策略已进入临床前及早期临床阶段:CCR2抑制剂可阻断单核细胞向肿瘤浸润;CSF1R抑制剂可耗竭M2型巨噬细胞;CD47-SIRPα轴阻断则恢复TAMs对肿瘤细胞的吞噬功能。此外,2026年3月,牛津大学Ester Hammond教授团队获得Brain Research UK资助,开展Ag5联合放疗治疗儿童高级别胶质瘤的研究。Ag5是一种银原子簇合物,可选择性升高肿瘤细胞活性氧(ROS)水平,使其突破耐受阈值而死亡,同时联合放疗产生协同杀伤效应。

图源:oncology.ox.ac.uk
展望:从单点突破到系统变革
当前胶质瘤研究已形成“物理开放屏障—精准靶向驱动—免疫协同激活—微环境重塑”的多维度治疗图谱。聚焦超声为药物进入打开物理通道,IDH1抑制剂为特定突变人群提供精准靶向,溶瘤病毒与免疫联合疗法突破“冷肿瘤”限制,AAV基因治疗开辟全新治疗范式。未来,随着多组学筛选、空间转录组学与个体化用药的进一步融合,基于患者肿瘤突变谱与微环境特征的组合治疗方案将逐步落地。
可以预见,胶质瘤治疗正从“手术+放化疗”的传统范式,迈向“物理破障+精准靶向+免疫激活+基因修饰”的系统性变革。这不仅是治疗手段的丰富,更是对“颅内不治”观念的颠覆。随着更多临床III期试验数据的读出,胶质瘤患者的长期生存希望正在从愿景走向现实。
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
