2025-2026糖尿病前沿研究荟萃:机制破局+靶点革新,引领精准诊疗新时代
糖尿病作为全球高发的慢性代谢性疾病,2型糖尿病占比超90%,长期面临胰岛素抵抗难逆转、并发症高发、个体化治疗不足等临床难题。
2025-2026年,糖尿病领域基础机制、临床诊疗、药物研发、全程管理多维度迎来前沿研究密集落地,彻底打破传统治疗局限,为糖尿病精准防控提供全新依据。

基础科研突破:
核心机制新发现,解锁干预新靶点
1.胰岛功能调控新机制:多分子通路实现精准修复
2026年1月,同济大学李维达、高绍荣团队在《Cell Research》发表重磅研究,揭示锌积累介导β细胞特性丧失的全新致病机制。
研究证实,糖尿病进展期胰岛内锌过载会触发综合应激反应(ISR),通过锌-ATF4-ARX调控轴,驱动功能性β细胞向α细胞转分化,直接引发胰岛素分泌不足。该研究借助人类胚胎干细胞衍生胰岛模型,不仅填补了人类β细胞退变机制空白,还证实抑制ISR、调控锌积累可有效保护β细胞特性、改善血糖控制,为胰岛功能修复与干细胞移植治疗糖尿病提供了全新靶点与干预方向。
图源:参考文献1
2.胰岛素抵抗机制新突破:组织特异性调控与菌群干预双管齐下
复旦大学附属中山医院团队建立全球首个2型糖尿病胰岛素抵抗四分型体系,通过多组学分析明确肝源性、肌源性、脂肪源性、多器官联合型抵抗的核心分子特征,针对性干预后血糖达标率较传统方案提升42%,彻底打破“一刀切”的抗抵抗治疗困境。
无独有偶,基于大型中东生物样本库开展的2型糖尿病分型研究也证实,不同种族人群的糖尿病亚型存在显著异质性,该研究通过临床表型、代谢特征与分子标志物联合分析,划分出中东人群特有的糖尿病亚型,进一步完善了全球糖尿病精准分型体系,为跨种族、个体化诊疗提供了关键依据,弥补了既往研究种族覆盖不全的短板。
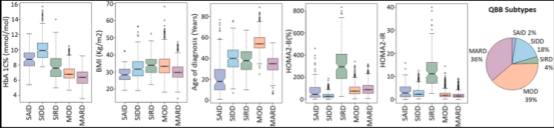
图源:参考文献2
3.并发症发生机制:多靶点明确,实现精准防护
糖尿病并发症是患者致残致死的核心原因,2026年多项前沿研究明确不同并发症的核心驱动机制,为靶向干预奠定基础:
• 糖尿病心肌病:重庆医科大学附属第一医院罗素新教授团队首次揭示异牡荆素(ISO)可通过促进SIRT3表达,抑制心肌细胞氧化应激损伤,使糖尿病模型小鼠心肌功能恢复55%以上,成为心血管并发症防护的潜在候选药物;
• 糖尿病视网膜病变:沈炜、宋洪元团队联合多家单位在《PNAS》发表研究,首次从全身角度揭示:高糖下单核细胞糖酵解亢进、组蛋白乳酸化升高,促使外泌体骨膜蛋白分泌,稳定缺氧诱导因子1α诱发新生血管,为糖网治疗提供全新靶点;
图源:参考文献3
• 糖尿病肾病:上海交通大学医学院团队证实,足细胞特异性蛋白Nephrin磷酸化异常是蛋白尿发生的核心机制,靶向激活该蛋白的小分子药物可减少糖尿病肾病患者尿蛋白排泄量40%以上。
图源:参考文献4
2026重磅研发与临床研究:
新药密集上市,管线成果亮眼
1.2026获批上市新药:靶点创新+剂型升级,覆盖全病程
药物/方案名称 | 研发企业 | 靶点/作用机制 | 适应症 |
司美格鲁肽超长效制剂 | 诺和诺德 | GLP-1受体激动剂 | 2型糖尿病;肥胖合并糖尿病 |
替尔泊肽口服剂型 | 礼来 | GLP-1R/GIPR双受体激动剂 | 2型糖尿病二线治疗 |
多格列艾汀片新适应症 | 华领医药 | 葡萄糖激酶激活剂(GKA) | 1型糖尿病联合胰岛素治疗 |
达格列净超长效制剂 | 阿斯利康 | SGLT-2抑制剂 | 2型糖尿病合并心衰/肾病 |
2.已上市药物:重塑高转移性卵巢癌治疗标准
(1) 多受体激动剂:从双靶点到三靶点,疗效再升级
礼来研发的GIP/GLP-1/GCGR三受体激动剂LY3437943公布III期临床数据,针对晚期2型糖尿病患者,HbA1c平均降低2.1%,减重率达15.6%,较双受体激动剂替尔泊肽疗效提升30%,同时可改善肝脏脂肪变性,为合并非酒精性脂肪肝的糖尿病患者提供新选择。
(2) 并发症靶向药物:精准干预,延缓病程
• 糖尿病视网膜病变:康弘药业研发的抗VEGF/Ang-2双抗眼内注射剂III期临床显示,每8周注射1次,视网膜新生血管消退率达82%,视力改善率较单靶点药物提升25%;
• 糖尿病周围神经病变:辉瑞研发的神经营养因子NGF激动剂PF-06753512II期临床证实,可显著改善肢体麻木、疼痛症状,有效率达78%,为神经病变患者缓解痛苦;
• 糖尿病心肌病:基于罗素新教授团队研究,异牡荆素肠溶制剂已进入I期临床,初步显示可降低糖尿病患者心肌氧化应激指标MDA水平40%,心肌保护效果显著。
参考文献
1. Ma Q, Xu W, Wang X, et al. Zinc accumulation-induced integrated stress response triggers β-cell identity loss. Cell Res. Published online January 28, 2026. doi:10.1038/s41422-026-01222-y
2. Al-Thani NM, Zaghlool SB, Toor SM, Abou-Samra AB, Suhre K, Albagha OME. Subtyping of type 2 diabetes from a large Middle Eastern biobank: Implications for precision medicine. Mol Metab. 2025;99:102195. doi:10.1016/j.molmet.2025.102195
3. Shen W, Nie Z, Wang M, et al. Monocyte-derived exosomal periostin driven by histone lactylation contributes to retinal neovascularization. Proc Natl Acad Sci U S A. 2025;122(44):e2501704122. doi:10.1073/pnas.2501704122
4. Yasuma T, Fujimoto H, D'Alessandro-Gabazza CN, et al. Microbiota-derived corisin accelerates kidney fibrosis by promoting cellular aging. Nat Commun. 2025;16(1):7591. Published 2025 Aug 25. doi:10.1038/s41467-025-61847-2
中洪博元动物模型——糖尿病
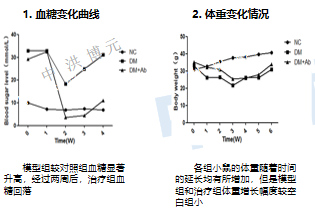
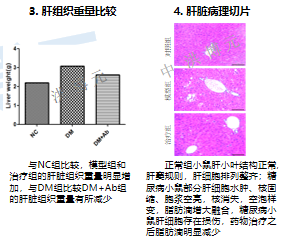
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
